- Operasi: automatik, PLC dikawal
- Utiliti: Untuk pengeluaran 1,000 Nm³/j H2daripada gas asli, Utiliti berikut diperlukan:
- 380-420 Nm³/j gas asli
- 900 kg/j air suapan dandang
- Kuasa elektrik 28 kW
- 38 m³/j air penyejuk *
- * boleh digantikan dengan penyejukan udara
- Hasil sampingan: eksport stim, jika diperlukan
Video
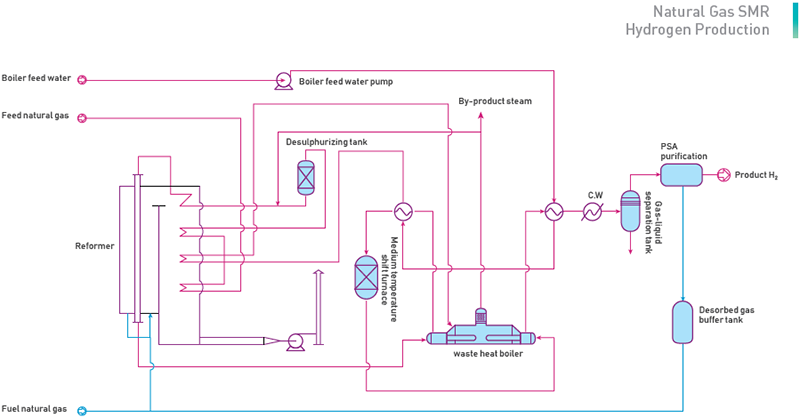
Pengeluaran hidrogen daripada gas asli adalah untuk melakukan tindak balas kimia gas asli bertekanan dan desulfur dan wap dalam reformer khas yang mengisi dengan mangkin dan menjana gas reforming dengan H₂, CO₂ dan CO, menukar CO dalam gas reforming kepada CO₂ dan kemudian mengekstrak. memenuhi syarat H₂ daripada gas-gas reforming melalui penjerapan ayunan tekanan (PSA).
Reka bentuk Loji Pengeluaran Hidrogen dan pemilihan peralatan terhasil daripada kajian kejuruteraan TCWY yang meluas dan penilaian vendor, dengan terutamanya mengoptimumkan perkara berikut:
1. Keselamatan dan Kemudahan operasi
2. Kebolehpercayaan
3. Penghantaran peralatan pendek
4. Kerja lapangan minimum
5. Modal dan kos operasi yang kompetitif
(1) Penyahsulfuran Gas Asli
Pada suhu dan tekanan tertentu, dengan gas suapan melalui pengoksidaan mangan dan zink oksida penjerap, jumlah sulfur dalam gas suapan akan dimatikan di bawah 0.2ppm di bawah untuk memenuhi keperluan pemangkin untuk pembaharuan stim.
Reaksi utama ialah:
| COS+MnO |
| MnS+H2O |
| H2S+ZnO |
(2) NG Steam Reforming
Proses pembentukan semula wap menggunakan wap air sebagai pengoksida, dan oleh pemangkin nikel, hidrokarbon akan diubah menjadi gas mentah untuk menghasilkan gas hidrogen. Proses ini adalah proses endotermik yang memerlukan bekalan haba daripada bahagian sinaran Relau.
Tindak balas utama dengan kehadiran pemangkin nikel adalah seperti berikut:
| CnHm+nH2O = nCO+(n+m/2)H2 |
| CO+H2O = CO2+H2 △H°298= – 41KJ/mol |
| CO+3H2 = CH4+H2O △H°298= – 206KJ/mol |
(3) Pemurnian PSA
Sebagai proses unit kimia, teknologi pemisahan gas PSA telah berkembang pesat menjadi disiplin bebas, dan semakin banyak digunakan dalam bidang petrokimia, kimia, metalurgi, elektronik, pertahanan negara, perubatan, industri ringan, pertanian dan perlindungan alam sekitar. industri, dsb. Pada masa ini, PSA telah menjadi proses utama H2pengasingan yang telah berjaya digunakan untuk penulenan dan pengasingan karbon dioksida, karbon monoksida, nitrogen, oksigen, metana dan gas industri lain.
Kajian mendapati bahawa beberapa bahan pepejal dengan struktur berliang yang baik boleh menyerap molekul bendalir, dan bahan penyerap tersebut dipanggil penyerap. Apabila molekul bendalir menghubungi penjerap pepejal, penjerapan berlaku serta-merta. Penjerapan menghasilkan kepekatan yang berbeza bagi molekul yang diserap dalam cecair dan pada permukaan penyerap. Dan molekul yang diserap oleh penyerap akan diperkaya pada permukaannya. Seperti biasa, molekul yang berbeza akan menunjukkan ciri yang berbeza apabila diserap oleh penjerap. Juga keadaan luaran seperti suhu bendalir dan kepekatan(tekanan)akan secara langsung mempengaruhi ini. Oleh itu, hanya disebabkan oleh ciri-ciri yang berbeza ini, dengan perubahan suhu atau tekanan, kita boleh mencapai pemisahan dan penulenan campuran.
Untuk tumbuhan ini, pelbagai bahan penjerap diisi di dalam katil penjerapan. Apabila gas reforming (campuran gas) mengalir ke dalam lajur penjerapan (katil penjerapan) di bawah tekanan tertentu, disebabkan oleh ciri-ciri penjerapan yang berbeza H2, CO, CH2, CO2, dsb. CO, CH2dan CO2diserap oleh penjerap, manakala H2akan mengalir keluar dari bahagian atas katil untuk mendapatkan hidrogen produk yang layak.










 MnS+CO2
MnS+CO2









